Таблица 10/1. Основные свойства аминокислотных остатков
| _____ Аминокислотный остаток _____ | % в белках E.coli | Мол вес при pH7 (дальтон) | DGвода®спирт
бок. группы при 250С (ккал/моль) |
||
| название | код | ||||
| 3-букв. | 1-букв. | ||||
| Глицин | Gly | G | 8 | 57 | 0 |
| Аланин | Ala | A | 13 | 71 | -0.4 |
| Пролин | Pro | P | 5 | 97 | -1.0 |
| Глутаминовая кислота | Glu | E | »6 | 128 | +0.9 |
| Глутамин | Gln | Q | »5 | 128 | +.03 |
| Аспарагиновая кислота | Asp | D | »5 | 114 | +1.1 |
| Аспарагин | Asn | N | »5 | 114 | +0.8 |
| Серин | Ser | S | 6 | 87 | +0.1 |
| Гистидин | His | H | 1 | 137 | -0.2 |
| Лизин | Lys | K | 7 | 129 | +1.5 |
| Аргинин | Arg | R | 5 | 157 | +1.5 |
| Треонин | Thr | T | 5 | 101 | -0.3 |
| Валин | Val | V | 6 | 99 | -2.4 |
| Изолейцин | Ile | I | 4 | 113 | -1.6 |
| Лейцин | Leu | L | 8 | 113 | -2.3 |
| Метионин | Met | M | 4 | 131 | -1.6 |
| Фенилаланин | Phe | F | 3 | 147 | -2.4 |
| Тирозин | Tyr | Y | 2 | 163 | -1.3 |
| Цистеин | Cys | C | 2 | 103 | -2.1 |
| Триптофан | Trp | W | 1 | 186 | -3.0 |
Примечания. Все данные взяты из [3], —
за исключением данных по гидрофобности боковых групп, которые взяты из
I.I.Fauchere, V.Pliska, Eur. J. Med. Chem.-Chim. Ther. (1983) 18:369.
Объем (в ![]() 3),
приходящийся на аминокислотный остаток в белке или в растворе, близок к
его молекулярному весу в (дальтонах), умноженному на 1.3. Точнее,
— процентов на 5 побольше, чем (мол. вес) x
1.3, если в остатке много алифатических (-СН2-,
-СН3) групп, и процентов на 5 поменьше,
чем (мол. вес) x 1.3, если
в остатке много полярных (О, N) атомов.
3),
приходящийся на аминокислотный остаток в белке или в растворе, близок к
его молекулярному весу в (дальтонах), умноженному на 1.3. Точнее,
— процентов на 5 побольше, чем (мол. вес) x
1.3, если в остатке много алифатических (-СН2-,
-СН3) групп, и процентов на 5 поменьше,
чем (мол. вес) x 1.3, если
в остатке много полярных (О, N) атомов.
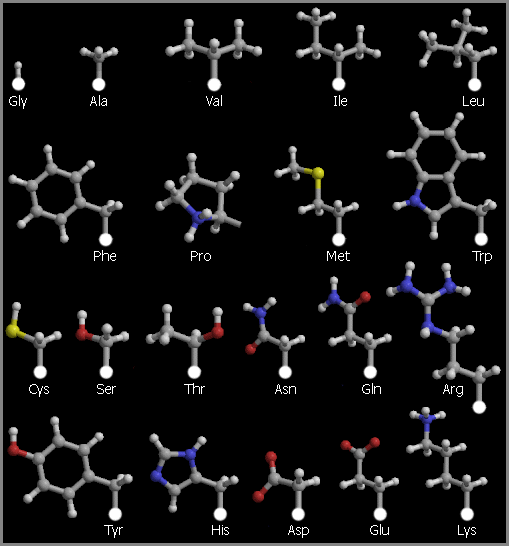
Рис.10-1. Боковые цепи двадцати
стандартных аминокислотных остатков.
Рассмотрим теперь структурные тенденции
аминокислотных остатков; они стали известными после многолетнего статистического
исследования белковых структур. Такие исследования отвечают на вопрос:
"Что чаще всего бывает, и чего чаще всего не бывает?".
Для систематизации ответов полезной
может быть следующая ниже Таблица 10/2, куда я вписал, наряду со встречаемостью
аминокислотных остатков в разных местах белков, такие свойства остатков,
как: наличие NH группы в главной цепи (ее нет только у иминокислоты пролина);
наличие Сb атома
в боковой цепи (его нет только у глицина); число не-водородных g
атомов в боковой цепи; наличие и вид полярных группировок в боковой цепи
(диполей или зарядов — со знаком; жирным выделено то зарядовое
состояние, что относится к "нормальному" рН7).
Таблица 10/2. Основные структурные свойства аминокислотных остатков
| A.к. | Наличие | число | Диполь/заряд | pK | Яркая тенденция быть в: | ||||||||
| ост. | NH | Cb | g | до | спираль | за | клубок | ядро | |||||
| aN | |aN | a | aC| | aC | b | ||||||||
| Gly | - | - | + | ||||||||||
| Ala | + | - | |||||||||||
| Pro | 1 | + | - | - | - | - | + | ||||||
| Glu | 1 | COOH Ю CO2- | 4.3 | + | + | - | - | - | - | ||||
| Asp | 1 | COOH Ю CO2- | 3.9 | + | + | - | - | - | - | + | - | ||
| Gln | 1 | OCNH2 | - | ||||||||||
| Asn | 1 | OCNH2 | + | - | + | - | + | - | |||||
| Ser | 1 | OH | + | + | |||||||||
| His | 1 | NH; и N Ю NH+ | 6.5 | - | + | + | |||||||
| Lys | 1 | NH2 Ю NH3+ | 10.5 | - | - | + | + | - | - | ||||
| Arg | 1 | HNC(NH2)2+ | 12.5 | - | - | + | + | - | + | - | |||
| Thr | 2 | OH | + | + | |||||||||
| Ile | 2 | + | - | + | |||||||||
| Val | 2 | + | - | + | |||||||||
| Leu | 1 | + | + | - | + | ||||||||
| Met | 1 | + | + | - | + | ||||||||
| Phe | 1 | + | - | + | |||||||||
| Tyr | 1 | OH Ю O- | 10.1 | - | + | + | |||||||
| Cys | 1 | SH Ю S- | 9.2 | - | + | + | |||||||
| Trp | 1 | NH | + | + | |||||||||
Попробуем понять основные закономерности этой таблицы исходя из того, что мы уже изучили. При этом мы будем использовать следующую логику: так как белок в целом стабилен — значит, он должен в основном состоять из стабильных элементов, т.е. именно они должны наблюдаться в его структуре чаще всего, а нестабильные должны наблюдаться редко.
Почему пролин не любит вторичной
структуры? — Потому, что у него нет NH-группы в главной цепи,
т.е. у него вдвое уменьшена возможность завязывать водородные связи
— а именно на них и держится вторичная структура. Почему он, тем
не менее, любит N-конец спирали? — Потому, что здесь, на N-конце,
NH-группы "торчат" из спирали — т.е. они и так не вовлечены
в водородные связи — и здесь пролину нечего терять...
С другой стороны, угол j в пролине фиксирован
его кольцом примерно при -60о —
т.е. его конформация уже почти "готова" для a-спирали
(Рис.10-2а).
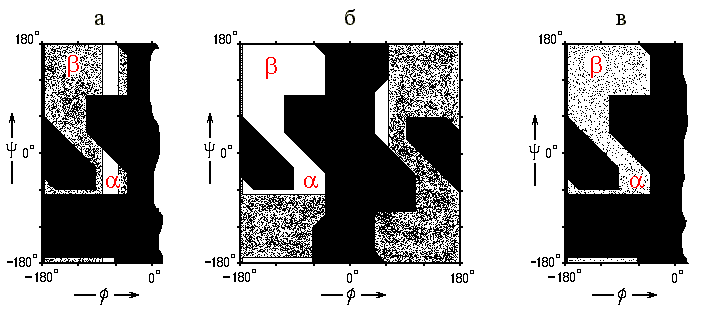
Рис.10-2. Запрещенные и разрешенные
конформации различных аминокислотных остатков и — на их фоне
— конформации a и b
структуры. (а) Разрешенные (![]() )
для пролина конформации на фоне конформаций, разрешенных для аланина (
)
для пролина конформации на фоне конформаций, разрешенных для аланина (![]() );
); ![]() — конформации, запрещенные для них обоих. (б) Разрешенные (
— конформации, запрещенные для них обоих. (б) Разрешенные (![]() )
конформации аланина на фоне конформаций
)
конформации аланина на фоне конформаций ![]() , разрешенные лишь для глицина;
, разрешенные лишь для глицина; ![]() — области, запрещенные для всех остатков. (в) Карта запрещенных (
— области, запрещенные для всех остатков. (в) Карта запрещенных (![]() )
и разрешенных (
)
и разрешенных (![]() ,
, ![]() )
конформаций более крупных остатков. В области
)
конформаций более крупных остатков. В области ![]() разрешены все конформации боковой группы по углу c1,
в области
разрешены все конформации боковой группы по углу c1,
в области ![]() часть углов c1
запрещена.
часть углов c1
запрещена.
Почему глицин не любит вторичной
структуры и предпочитает нерегулярные участки ("клубок")? —
Потому, что для него допустима очень широкая область углов (jy)
на карте Рамачандрана (Рис.10-2б), — ему легко принимать самые
разнообразные конформации, лежащие вне вторичной структуры.
Наоборот, аланин —
с более узкой, но включающей и a, и b
конформацию разрешенной областью на карте Рамачандрана (Рис.10-2б)
— предпочитает нерегулярным конформациям a-спираль
(и отчасти b-структуру).
Остальные гидрофобные остатки
(т.е. остатки без зарядов и диполей в боковой цепи) предпочитают, как правило,
b-структуру. Почему? Потому, что их крупные
g-атомы могут там располагаться более свободно
(Рис.10-2в). Особенно это важно для боковых групп с двумя крупными g-атомами
— и, действительно, они любят b-структуру
особенно сильно.
А вот аминокислоты с полярными
группами в боковых цепях предпочитают нерегулярные участки ("клубок"),
где эти полярные группы могут завязать водородные связи. Особенно заметна
эта тенденция для наиболее полярных, заряженных при "нормальном" рН7 остатков,
и для самых коротких (см. Рис.10-1), наиболее приближенных к главной цепи
полярных боковых цепей. Кстати, по той же причине, — поскольку
у них там есть возможность завязать дополнительную водородную связь,
— короткие полярные боковые группы любят места у обоих концов спирали.
Некое исключение среди аминокислот
с диполями в боковой цепи составляют триптофан и тирозин, имеющие маленький
диполь на фоне большой гидрофобной части, и цистеин, у которого (т.е. у
SН-группы которого) водородные связи совсем слабые. Они ведут себя, в общем,
так же, как гидрофобные остатки.
Мы видим также, что отрицательно
заряженные боковые группы предпочитают N-конец спирали (точнее:
N-концевой виток и один-два остатка перед ним) и не любят С-концевой виток
(и пару остатков за ним), а положительно заряженные — предпочитают
C-конец спирали и не любят ее N-конец. Почему? — Потому, что на N-конце
из спирали торчат NH-группы и на нем образуется заметный положительный
заряд, и "минусы" боковых цепей притягиваются к нему, а "плюсы" —
отталкиваются от него (Рис.10-3). А С-конец спирали заряжен, наоборот,
отрицательно, — и там эффект противоположен: около С-конца
любят собираться "плюсы" боковых цепей, а "минусы" его избегают.
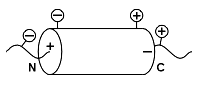 Рис.10-3.
Рис.10-3. Что касается расположения остатков
внутри белка или на его поверхности — здесь общая тенденция
заключается в том, что полярные (гидрофильные) боковые группы находятся
снаружи, где они могут контактировать с полярной же водой ("подобное растворяется
в подобном"!). Отрываться от воды полярным группам плохо —
теряются водородные связи. Особенно плохо отрываться заряженным группам:
переход из среды с высокой диэлектрической проницаемостью (из воды) в среду
с низкой (ядро белка) ведет к большому повышению свободной энергии. И действительно,
— ионизированных групп внутри белка практически нет (а почти все
исключения связаны с активными центрами — ради которых, собственно,
белок и создан...).
Наоборот, большинство гидрофобных
боковых групп находятся внутри белка — они-то и создают здесь
гидрофобное ядро (опять: "подобное растворяется в подобном"!). Мы уже говорили,
что гидрофобность группы тем больше, чем больше ее неполярная поверхность:
именно ее нужно упрятать от воды. Для чисто неполярных групп гидрофобный
эффект прямо пропорционален их поверхности, а для групп с полярными вкраплениями
— их поверхности, за вычетом поверхности этих вкраплений.
Слипание гидрофобных групп
— главная движущая сила образования белковой глобулы. Главная,
но не единственная — еще есть образование водородных связей
во вторичной структуре (о чем мы уже говорили) и образование плотной, квазикристаллической
упаковки внутри белка (о чем мы еще поговорим в свое время).
Для создания гидрофобного ядра
белковой цепью, она должна входить в него с уже насыщенными водородными
связями — ведь иначе ее полярным пептидным группам от воды
придется оторваться, а разрыв водородной связи дорог. Поэтому в гидрофобное
ядро вовлекается цепь, уже образовавшая (или образующая при этом) вторичную
структуру и тем самым насытившая водородные связи пептидных групп в главной
цепи. Однако при этом в ядро должны увлекаться только гидрофобные остатки
вторичной структуры, а входящие в нее полярные остатки должны остаться
вне ядра, — потому и на a-спиралях,
и на b-структурных участках выделяются гидрофобные
и гидрофильные поверхности; для их создания необходимо определенное чередование
соответствующих групп в белковой цепи (Рис.10-4).
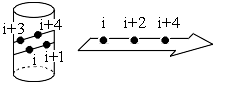
Рис.10-4. Боковые группы, которые
(если все они — неполярные) могут формировать единые гидрофобные
поверхности на a-спиралях и на b-структурных
участках. Аналогичные сочетания полярных групп в цепи приводят к образованию
гидрофильных областей на противоположных поверхностях на a-спиралей
и на b-тяжей.
Все закономерности, о которых мы сейчас говорили, используются как для конструирования искусственных белков, так и для предсказания — по аминокислотным последовательностям — вторичной структуры белков, а также для предсказаний тех участков их цепи, что глубоко погружены в белок, — или, наоборот, тех участков, что лежат на поверхности белка. К этим вопросам мы еще вернемся.
В заключение — еще
немного о заряженных (или, точнее, ионизуемых) боковых группах. Повышение
рН всегда делает группу "более отрицательной" — нейтральная
группа приобретает отрицательный заряд, а положительно заряженная
— разряжается, см. Рис.10-5. Переход из незаряженного в заряженное
или из заряженного в незаряженное состояние происходит у разных групп при
разных рН, однако ширина перехода при этом всегда одна и та же —
около 2 единиц рН (в этом интервале отношение заряженной и незаряженной
форм меняется от 10:1 до 1:10).
Следует обратить особое внимание
на группы, переходящие из незаряженного в заряженное состояние при рН близком
к 7, характерном для жизни белка в клетке: именно такие легко перезаряжаемые
группы (и особенно гистидин) часто используются в активных центрах белков.
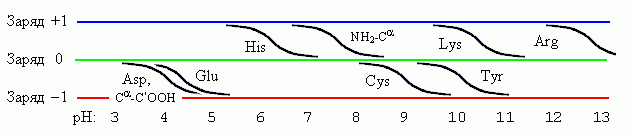
Рис.10-5. Заряженность ионизуемых
боковых групп, а также N-конца пептидной цепи (NH2-Ca)
и ее С-конца (Ca-C'OOH)
при разных рН.