Рассмотрим сначала фибриллярные белки.
Фибриллярные белки играют в основном
структурную роль. Они образуют микрофиламенты, микротрубочки, —
а также фибриллы, волосы, шелк и другие защитные покровы; они армируют
мембраны и поддерживают структуру клеток и тканей.
Фибриллярные белки часто образуют
огромные агрегаты; их пространственная структура высоко регулярна, сложена
в основном из очень больших блоков вторичной структуры, и держится в значительной
степени на взаимодействии между разными полипептидными цепями. Первичная
структура фибриллярных белков также высоко регулярна, периодична,
— потому-то из нее и образуется обширная регулярная вторичная структура.
Типичными представителями фибриллярных белков являются:
а) b-структурный
белок фиброин шелка. У b-листа, как мы знаем,
периодичность состоит в чередовании остатков, обращенных "вверх" и "вниз"
(Рис.11-1).
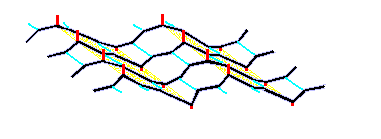
Соответственно, в фиброине шелка
основной мотив первичной структуры выглядит как повтор восьми блоков, где
в каждом из блоков идет чередование маленьких (Gly) и более крупных остатков,
например:
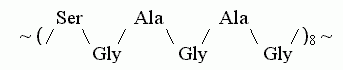 ,
,
и этот восьмикратный повтор шести остатков повторяется около 50
раз.
Антипараллельные (такие, как на
Рис.11-1) b-слои фиброина шелка уложены друга
на друга по принципу "лицом к лицу, спина к спине": двойной слой глицинов
(расстояние между плоскостями — 3.5![]() )
— двойной слой аланинов/серинов (расстояние между плоскостями
— 5.7
)
— двойной слой аланинов/серинов (расстояние между плоскостями
— 5.7![]() ;
это хорошо видит рентген) — двойной слой глицинов —
и т.д.
;
это хорошо видит рентген) — двойной слой глицинов —
и т.д.
б) a-структурные
фибриллярные белки, сложенные из длинных перевитых спиралей (coiled coil)
(Рис.11-2). В a-кератине или тропомиозине такие
спирали охватывают всю белковую цепь, — да и большая часть
миозиновой цепи образует фибриллу такого типа. Такие структуры содержатся
также в шелке — но не обычном шелке тутового шелкопряда, а
шелке пчел и муравьев.
Слипаясь, отдельные цепи образуют
суперспираль.
|
Рис.11-2. Перевитые правые a-спирали. В комплексе
они лежат параллельно друг другу и слегка закручены одна вокруг другой
так, что каждая из них образует левую суперспираль. Контактирующие аминокислотные
остатки занимают в цепи позиции a и d (см. Рис.11-3, 11-4).
|
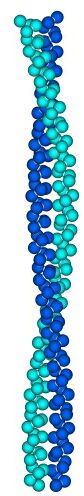 |
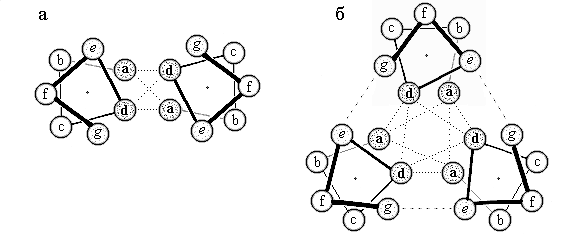
Рис.11-3. Взаимодействие a-спиралей
в двойной (а) и тройной (б) суперспирали (вид с торца спирали). В двойной
суперспирали непосредственно контактируют с другой спиралью только остатки
а и d, а в тройной — еще и остатки e и
g (хотя и более слабо).
На следующем структурном уровне
изображенные на Рис.11-2 суперспирали часто (но не всегда —
например, не в тропомиозине) слипаются друг с другом и образуют фибриллы.
Входящие в суперспираль a-спирали
обычно параллельны, и перевиты они — в разных белках
— по две, три или четыре. У a-спирали,
как мы уже знаем, период равен 3.6 остатка на виток. В перевитых спиралях
периодичность — 7 остатков на два витка a-спирали,
т.е. 3.5 остатка на виток (Рис.11-3, 11-4).
Типичная первичная структура при
этом выглядит, как на Рис.11-4.
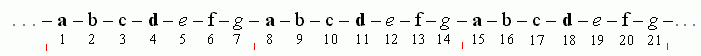 Рис.11-4.
Рис.11-4.На этом рисунке жирные буквы соответствуют гидрофобным (жирным, слипающимся) аминокислотам, а прочие буквы — аминокислотам гидрофильным. Интересно, что небольшое увеличение гидрофобности остатков e и g превращает двойную перевитую спираль (Рис.11-3а) в тройную (Рис.11-3б), а еще большее — в четверную.
Остановимся чуть подробнее на том,
как спирали слипаются между собой. На a-спирали
(Рис.11-5, слева) есть несколько спиральных нарезок — "хребтов"
из сближенных в пространстве боковых групп. Одни хребты имеют периодичность
типа 1 — 4 — 7 — ... , и та их часть, что
входит в зону контакта, состоит из пар a1
— d4, a8
— d11, ... (Рис.11-5, в центре).
Другие хребты имеют периодичность типа 0 — 4 —
8 — 12 — ... . Та часть этих хребтов, что входит в зону
контакта, состоит из пар d4
— a8, d11
— a15, ... (Рис.11-5, справа).
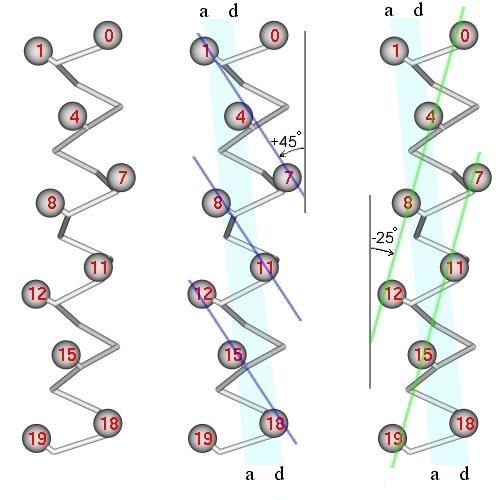
Первые хребты (если проводить их
через выступы, образованные боковыми группами) идут под углом примерно
25о к оси спирали, вторые —
под углом примерно 45о (Рис.11-5б и 11-5в).
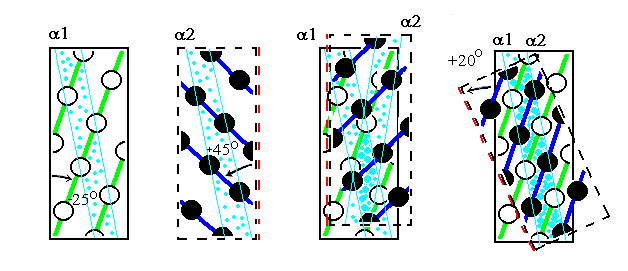
Если, перевернув вокруг вертикальной оси, наложить одну поверхность на
другую (Рис.11-6, слева), а затем повернуть на 20о
вокруг вертикальной оси, — то хребты типа "1 —
4 — 7" одной спирали окажутся между хребтами типа "0
— 4 — 8" другой, что обеспечит их плотный контакт (Рис.11-6,
справа). При этом группы а одной спирали окажутся между группами
d другой, а зона контакта образует на поверхности обеих спиралей
(пока они не суперспирализованы) слабо скрученную спиральную полосу. А
когда эти спирали суперспирализуются (Рис.11-2) и обовьются вокруг общей
оси — зона контакта окажется в центре слегка перевитого пучка.
Это — не единственный способ плотного контакта спиралей (с другими мы познакомимся, когда будем говорить о глобулярных белках), — но единственный, пригодный для очень длинных спиралей, типичных для фибриллярных белков. Он был предсказан еще Криком в том же 1953 году, когда он — вместе с Уотсоном — предсказал двойную спираль ДНК.
в) Коллаген. Главный опорный белок.
Он образуется особой, тройной суперспиралью, сложенной из трех полипептидов
(Рис.11-7). При этом внутри каждого полипептида, внутри каждой нити этой
тройной спирали водородных связей нет — они есть только между
нитями.
Конформация всех остатков в каждой
цепи коллагена близка к конформации полипролиновой [точнее —
poly(Pro)II] спирали. Это — левая спираль, и период ее равен
трем. Соответственно, основной мотив первичной структуры в коллагене выглядит
как многократный повтор троек (Gly-Pro-Pro)n,
или, точнее, (Gly-нечто-Pro)n, причем Gly
в такой тройке необходим для образования водородных связей: у него есть
NH-группа (в отличие от Pro), и нет боковой группы, — а любая
боковая группа была бы лишней в центре тугой коллагеновой спирали, где
сидит глицин.
Интересно, что экзоны, кодирующие
коллагеновую цепь, всегда начинаются с глицинов и всегда содержат число
кодонов, кратное трем. Я надеюсь, вы помните, что гены эукариот содержат
экзоны, кодирующие белки, и интроны, которые выщепляются из матричной РНК
(и потому белки не кодируют).
|
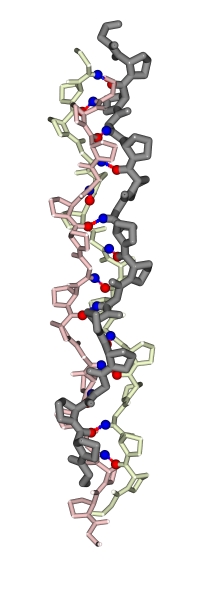
Рис.11-7. Модель тройной суперспирали коллагена для последовательности
(глицин — пролин — пролин)n.
Каждая цепь выделена своим цветом. Отмечены завязывающие водородные связи
Н-атомы NH-групп глицина (синим) и О-атомы СО-групп первого пролина тройки
Gly-Pro-Pro (красным). При этом Gly цепи "1" завязывает связь с цепью "2",
а Pro — с цепью "3", и т.д. Завиваясь вокруг двух других, каждая
цепь коллагена образует правую суперспираль. "Супер" —
потому что на более мелком масштабе, на масштабе конформаций отдельных
остатков, коллагеновая цепь уже образует спираль типа poly(Pro)II (причем
эта "микроспираль" — левая); ее можно проследить по
направлению пролиновых колец.
|
 |
На следующем структурном уровне, коллагеновые суперспирали также слипаются друг с другом и образуют фибриллы коллагена.
Биосинтез коллагена, его последующая
модификация и образование зрелой структуры коллагеновой фибриллы хорошо
изучены (Рис.11-8). Замечу, что сам по себе коллаген не способен
к спонтанной и при этом правильной самоорганизации своей пространственной
структуры in vitro — так же, как и фиброин шелка,
— и в отличие от глобулярных белков, о которых я буду говорить потом.
Для самоорганизации нужен проколлаген, включающий, кроме коллагеновых
нитей, глобулярные головки и хвостики. Лишенные головок и хвостиков коллагеновые
нити, самоорганизуясь из развернутого состояния in vitro, тоже складываются
в тройные спирали — но "неправильные", без присущей нативному
коллагену гетерогенности тройной спирали (включающей нити двух сортов),
без присущего ему регистра (т.е. с неправильным сдвигом нитей относительно
друг друга), и т.д.
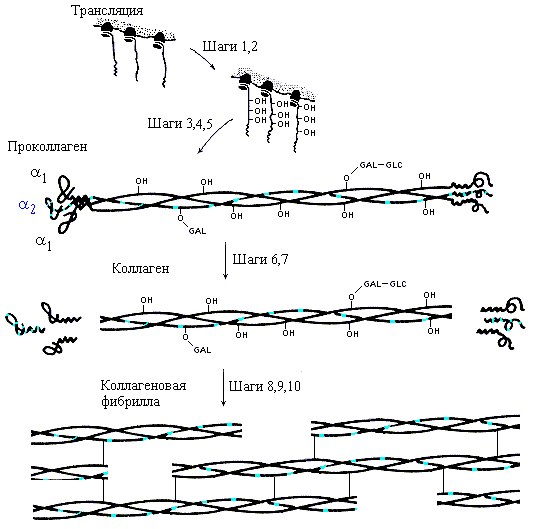
Рис.11-8. Образование коллагена
in vivo. Шаг 1. Биосинтез про-a1-цепей
и про-a2-цепей
(по 1300 остатков в каждой) в пропорции 2:1. Шаг 2. Гидроксилирование
некоторых остатков Pro и Lys. Шаг 3. Присоединение сахаров (GLC-GAL)
к гидроксилированным остаткам. Шаг 4. Образование тримера и SS связей
на его концах. Шаг 5. Образование тройной спирали в середине проколлагена.
Шаг 6. Секреция проколлагена во внеклеточное пространство. Шаг
7. Отщепление глобулярных частей. Шаги 8-10. Спонтанное образование
фибрилл из тройных суперспиралей, окончательная модификация аминокислотных
остатков и образование ковалентных сшивок модифицированных остатков коллагеновых
цепей. Картинка взята из [3] и адаптирована.
В заключение, я хочу подчеркнуть,
что фибриллярные белки устроены относительно просто в силу периодичности
своей первичной и, в силу этого, — также и своей вторичной
структуры.