Начнем с a-спиралей.
Первая водородная связь в ней, (СО)0
— (HN)4, фиксирует конформации трех
остатков — 1, 2, 3; следующая водородная связь, (СО)1
— (HN)5, дополнительно фиксирует
конформацию только одного остатка — остатка 4; связь (СО)2
— (HN)6 дополнительно фиксирует остаток
5, и т.д.
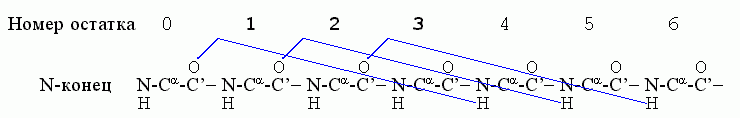
Значит, если в спирали фиксировано
n остатков, то их фиксирует n-2 водородные связи. Рассмотрим
свободную энергию образования такой спирали из клубка в водном окружении
("клубок" — это полимер без структуры и без взаимодействия
дальних по цепи звеньев). Эту свободную энергию можно записать как
| DFa = Fa — Fклуб. = (n-2)fH — nTSa = -2fH + n(fH —TSa) | (9.1) |
Здесь fH — свободная энергия
водородной связи в a-спирали (вы помните, что
fH — не просто энергия, как
было бы в вакууме: в нее входит и энергия, и энтропия перестроек водородных
связей в водном окружении), а Sa
— потеря энтропии при фиксации одного остатка в спирали.
Вы видите, что в DFa
есть два члена. Один (-2fH) не зависит
от длины спирали; величина
| fINIT = -2fH | (9.2) |
традиционно называется свободной энергией инициации спирали (на самом деле, fINIT
— суммарная свободная энергия обеих границ спирали с клубком
— учитывает и инициацию, и терминацию спирали). Другой член,
n(fH-TSa),
прямо пропорционален длине спирали; величина
| fEL = (fH-TSa) | (9.3) |
называется свободной энергией элонгации спирали на один остаток. В общем
виде,
| DFa = fINIT + n.fEL . | (9.4) |
При этом отношение вероятности чисто спирального состояния цепи из n
остатков к ее же чисто клубковому (и начисто лишенному спиральных примесей)
состоянию, равно
| exp(-DFa/kT) = exp(-fINIT/kT).[exp(-fEL/kT)]n = ssn | (9.5) |
Здесь я использовал общепринятые обозначения:
— фактор элонгации спирали:
s = exp(-fEL/kT);
— фактор инициации спирали:
s = exp(-fINIT/kT);
ясно, что s<<1, так как s
= exp(-fINIT/kT) = exp(+2fH/kT);
а свободная энергия водородной связи — большая отрицательная
величина, порядка нескольких kT.
Прежде, чем говорить о том, как экспериментально определяются величины s и s, — выясним общий вопрос о том, как образуется спираль при изменении условий среды (температуры, растворителя и т.д.) — переходом "все-или-ничего" или постепенно?
Поначалу кажется, что такая отличная
от клубка структура, как спираль, должна "вымораживаться" из него путем
фазового (т.е. "все-или-ничего") перехода — как лед из воды...
Однако на этот счет есть теорема
Ландау, которая гласит, что в системе, где обе фазы одномерны,
— фазовый переход первого рода невозможен. Попытаюсь объяснить эту
теорему.
Прежде всего — что
значит "одномерность". Это значит, что размер границы, "стыка" фаз не зависит
от размера кусков этих фаз. В этом смысле и спираль, и клубок в полимере
— одномерны. Рисунок 9-1 поясняет, что граница (стык) спирали и клубка
не зависит ни от длины спирали, ни от длины клубка, — в то
время как поверхность, граница трехмерной фазы (например, льдинки в воде)
зависит от ее размера. Соответственно, свободная энергия границы спирали
и клубка не зависит от их длин, а свободная энергия поверхности трехмерной
фазы растет как n2/3 с ростом числа
n вовлеченных в нее частиц.
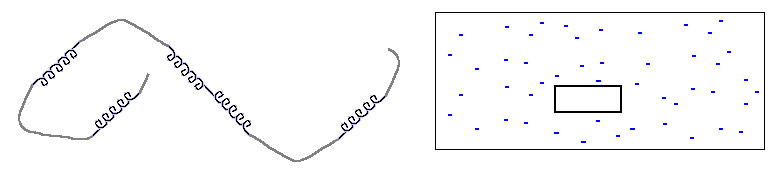
Рис.9-1. Сравнение одномерной
(клубок со спиралями) и трехмерной (льдинка в воде) систем. Размер стыка
спирали и клубка не зависит их длин; поверхность трехмерной льдинки зависит
от ее размера.
Теперь — что значит
"происходит как фазовый переход первого рода". Это значит, что при температуре
перехода стабильной может быть либо одна, либо другая фаза, но перемешивание
фаз (например, льда и воды) ведет к повышению свободной энергии, и потому
нестабильно. Здесь вас не должна вводить в искус картина плавающего в воде
льда: при любой температуре такое состояние неустойчиво (из-за повышенной
свободной энергии на границе воды со льдом), и со временем лед или растает,
или охватит всю воду — конечно, если нет тока подземного тепла,
течений и других неравновесных вещей...
Выгодно ли сосуществование фаз
в трехмерной системе? Нет. Почему? Обратимся опять к Рис.9-1. Рассмотрим
температуру, где безграничная вода и безграничный лед имеют равную свободную
энергию (это и есть условие "точки перехода"). Если в воде плавает льдина
из n молекул, свободная энергия границы пропорциональна xn2/3,
где n2/3 — характерное
число пограничных молекул, а x>0 —
энергия границы в расчете на одну из них. (Замечание. Если x<0,
"перемешивание" — оно при этом всегда термодинамически выгодно
— произойдет на молекулярных масштабах, и двух фаз не будет вообще).
Значит, поверхность льдинки повышает свободную энергию на xn2/3.
Правда, льдинка имеет еще позиционную энтропию, так как может находиться
в разных точках сосуда. Но эта энтропия не превосходит величину порядка
k. ln(N), если в сосуде — всего
N молекул (т.е. N точек, с которых может начинаться льдинка). Итого
— свободная энергия льдинки — порядка [xn2/3
- kТ.ln(N)]. Но логарифм —
очень "слаборастущая" при больших N функция. Если льдинка занимает заметную
часть сосуда (скажем, n~N/10), и N очень велико [скажем, 10 000
000 000], то ln(N) [в данном случае - 23] очень мал по сравнению с (N/10)2/3
[в данном случае - с 1 000 000], — то есть в свободной энергии
льдинки доминирует граничный член xn2/3,
а он противится ее образованию... Поэтому в трехмерной системе макроскопические
фазы разделяются ("льдинки" из нескольких молекул — не в счет:
это просто микроскопические, локальные флуктуации), и фазовый переход первого
рода в ней возможен.
А выгодно ли сосуществование фаз
в одномерной системе? Оказывается, да. Рассмотрим опять температуру
"середины перехода", где спираль и клубок имеют равную свободную энергию,
т.е. где fEL=0. Свободная энергия обеих
границ спирали и клубка, fINIT, не зависит
ни от размера спирали, ни от размера клубка. Позиционная энтропия спирали
длины n в цепи длины N равна k.ln(N-n).
Итого, свободная энергия этой плавающей спирали есть fINIT
- kТ.ln(N-n). При больших
N, член с ln(N-n) всегда доминирует в этом выражении, даже
если n ~ 0.9 N; а этот логарифмический член понижает свободную энергию
и способствует внедрению спирали в клубок (и, точно так же, —
клубка в спираль)... Поэтому в одномерной системе фазы не разделяются,
они стремятся перемешаться, — а раз так, то и фазовый переход
первого рода (или типа "все-или-ничего") невозможен —
при достаточно большой длине цепи. Теорема Ландау доказана.
Теперь можно поставить вопрос
— при каких характерных длинах цепи начинается смешение клубковой
и спиральной фаз?
Рассмотрим цепь из N звеньев при
температуре "середины перехода", где спираль и клубок имеют равную свободную
энергию, т.е. fEL=0. При этом свободная
энергия элонгации спирали (а равно и клубка) — ноль, ее инициации
— fINIT, а число возможных положений
спирали в цепи из N звеньев — порядка N2/2
(она может начинаться и кончаться в любом месте при единственном условии,
что ее длина — не менее трех остатков); и ни расположение спирали
в цепи, ни ее длина (при fEL=0) не влияют
на ее свободную энергию. Для получения качественной оценки —
пренебрежем мелочами (цифрами) по сравнению с главным (буквами). Итак:
размещений спирали — порядка N2,
т.е. их энтропия — k x
2ln(N), а полная свободная энергия внедрения куска новой фазы (спирали
с флуктуирующими концами) в цепь длины N — примерно fINIT
- 2kТ.ln(N). Если она, эта
свободная энергия, больше нуля — новая фаза не внедрится; если
она меньше нуля — новая фаза может внедриться неоднократно.
Значит, смешение клубковой и спиральной фаз начинается в кусках длины N
~ n0, а величина n0
получается из уравнения fINIT - 2kТ.ln(n0)
= 0. Итак: характерная длина кусков спирали и клубка в середине перехода
| n0 = exp(+fINIT/2kТ) = s - 1/2 . | (9.6) |
Точка (температура) середины перехода
на опыте находится как та точка, где спиральность очень длинного полипептида
составляет 50% (спиральность обычно измеряют при помощи КД спектров, как
о том говорилось выше; при 50% спиральности КД спектр полипептида выглядит
как полусумма спектров клубкообразного полипептида и полипептида, спирального
на 100%). В этой точке fEL=0, т.е. s =
exp(-fEL/kT) = 1.
Измеряя в тех же условиях (когда
s=1) зависимость спиральности от длины полипептида, можно найти n0,
— как ту длину цепи, при которой ее средняя степень спиральности
в 4 раза меньше, чем у очень длинной цепи (т.е. чем 50%).
Точный расчет и
доказательство того, что цепь из n0 = s
-1/2 звеньев имеет именно (1/4) 50% = 12% спиральности
при s=1, — выходит за рамки нашего курса. Однако получить приблизительную
оценку нетрудно. В самом деле, в цепи из n0 звеньев сумма
вероятностей всех состояний, включающих a-спираль,
близка — по определению — к 50%. А так как состояние "со спиралью"
обычно имеет вид типа "клубок_на_одном_конце_цепи — спираль
— клубок_на_другом_конце_цепи", то, в среднем, эта спираль
— если она есть вообще (а вероятность этого "вообще" —
50%) — включает 1/3 звеньев цепи. Итого
— средняя спиральность цепи из n0 звеньев
приближенно равна 50% x (1/3)
= 17%.
Наконец, зная n0,
— можно вычислить fINIT и s.
Для большинства аминокислот n0 »
30, fINIT »
4 ккал/моль, и s » 0.001.
Теперь мы можем найти свободную энергию образования водородной связи (вкупе со всеми сопутствующими образованию Р-связи в a-спирали взаимодействиями): согласно (9.2), fH = -fINIT/2 » -2 ккал/моль. Можно найти и конформационную энтропию, теряемую при фиксации одного звена в a-спирали: согласно формуле (9.3), TSa = fH » 2 ккал/моль.
Оба параметра стабильности спирали
— и fEL, и fINIT
— зависят от температуры, но по-настоящему сильно влияет на стабильность
спирали именно отклонение величины fEL
от 0. Дело в том, что в спирали, состоящей из ~n0
звеньев, это отклонение умножается на большое число n0
— и уже в таком виде входит в свободную энергию спирали. Когда величина
fELxn0/kT
составляет порядка +1 (более точная оценка: fELxn0/kT
= +2), спиральность практически исчезает, а когда fELxn0/kT
= -2, — практически исчезает клубок. Значит, при n0»30,
переход спираль-клубок в очень длинных (N>>n0)
полипептидных цепях происходит в области -0.07 < fEL/kT
< 0.07 (Рис.9-2). Это — пример резкого, кооперативного,
— но не фазового (т.к. ширина его не стремится к нулю
по мере роста длины цепи) перехода.
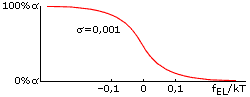
Рис.9-2. Переход спираль-клубок
всегда — даже для бесконечно длинных цепей — имеет
конечную ширину. Это — пример не фазового, но кооперативного
перехода: при малой величине фактора инициации спирали (s<<1)
он совершается при совсем небольшом (много меньше, чем на kT) изменении
величины fEL, — что показывает,
что "единица перехода" кооперирует много звеньев цепи, — но
отнюдь не всю эту цепь.
Для измерения влияния отдельных
аминокислотных остатков на стабильность спиралей сейчас чаще всего используются
короткие (длиной ~n0 или менее) полипептиды.
В них может образоваться только одна спираль, и оценить влияние каждой
аминокислотной замены на спиральность здесь наиболее просто. Сейчас известно,
что вклад аминокислотного остатка в стабильность спирали лежит в следующих
пределах: аланин; самый "спиралеобразующий" остаток: s »
2, т.е. fEL »
-0.4 ккал/моль; глицин, самый "спиралеразрушающий" остаток: fEL
» +1 ккал/моль, т.е. s »
0.2; правда, у пролина — иминокислоты (не имеющей NH
группы, которая должна завязывать структурообразующую водородную связь
в a-спирали) — у него величина s
еще много меньше, порядка 0.01 — 0.001, но точно она еще не
измерена.
Ранее аналогичные оценки делались,
используя статистические сополимеры (например — цепи, включающие
случайным образом перемешанные 80% Glu и 20% Ala), и именно так были получены
первые — а значит, и самые важные оценки, но с появлением возможности
синтеза полипептидов с заданной последовательностью — такие
работы на случайных сополимерах, видимо, отошли в прошлое.
Используя короткие пептиды с заданной
первичной структурой, можно даже оценить влияние на спиральность каждой
точечной аминокислотной замены в каждом конкретном месте такого пептида
— т.е., фактически, в зависимости от расположения аминокислотного
остатка относительно N- и С-концов спирали. Боковые группы взаимодействуют
с этими концами по-разному — в частности, заряженные группы,
потому что на N-конце спирали, как уже говорилось, сидят свободные от водородных
связей NH-группы главной цепи (и парциальный заряд N-конца a-спирали
равен +e/2), а на другом ее конце — СО-группы (с суммарным
парциальным зарядом в половину электронного, — -e/2).
Кроме того, для измерения стабильности
спирального состояния (величины fEL) в
полипептидах, включающих кислотные или осн![]() вные
боковые группы (например, в поли(Glu) или поли(Lys)), используется потенциометрическое
титрование. Идея этого подхода — в том, что заряжая спираль,
мы разрушаем ее (т.к. в спирали заряды боковых групп более сближены и потому
сильнее расталкиваются), — так что стабильность спирали можно
рассчитать, зная, как суммарный заряд цепи зависит от рН среды. К сожалению,
более подробное рассмотрение этого интересного метода выходит за рамки
данного курса.
вные
боковые группы (например, в поли(Glu) или поли(Lys)), используется потенциометрическое
титрование. Идея этого подхода — в том, что заряжая спираль,
мы разрушаем ее (т.к. в спирали заряды боковых групп более сближены и потому
сильнее расталкиваются), — так что стабильность спирали можно
рассчитать, зная, как суммарный заряд цепи зависит от рН среды. К сожалению,
более подробное рассмотрение этого интересного метода выходит за рамки
данного курса.
Аналогичные подходы применяются и для измерения стабильности b-структуры в полипептидах. Однако они менее развиты, так как b-структура сильно агрегирует. Сейчас стабильность b-структуры часто измеряют прямо в белке — путем оценки влияния на его стабильность точечных замен отдельных, лежащих на его поверхности b-структурных аминокислотных остатков. Способность разных остатков стабилизировать b-структуру мы рассмотрим на следующей лекции.
Рассмотрим теперь скорость образования вторичной структуры в пептидах.
a-спирали
образуются быстро — показано, что за десятую долю микросекунды
спираль охватывает пептид из 20-30 остатков (для столь быстрых измерений
приходится греть раствор пико— или наносекундным лазерным ударом).
Значит, спирали нарастают со скоростью по крайней мере порядка 1 остаток
за несколько наносекунд.
Я сказал "по крайней мере", так
как скорость образования спирали зависит не только от скорости, с которой
она нарастает, но и от скорости, с которой в цепях появляются первые зародыши
спиральной структуры. А инициация спирали требует преодоления активационного
барьера — и потому образование первого витка спирали требует
много больше времени, чем ее последующее удлинение еще на один виток. Так
что возможно, что элонгация спирали идет много быстрее, а все наблюдаемое
время тратится на ее инициацию. Разберемся в этом вопросе чуть внимательнее.
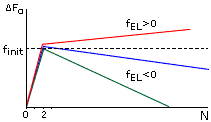
Рис.9-3. Характерная зависимость
свободной энергии спирали (DFa)
от числа вовлеченных в нее аминокислотных остатков (N) при разных свободных
энергиях ее элонгации (fEL). При fEL<0
— длинная спираль стабильна, но ее образование требует инициации,
— преодоления активационного барьера высотой fINIT.
При fEL>0 — спираль любой длины
нестабильна и, следовательно, не образуется.
Характерная зависимость свободной
энергии спирали от ее длины показана на Рис.9-3. Даже когда fEL<0
— т.е. когда достаточно длинная спираль стабильна —
образование первого витка в ней требует преодоления активационного барьера
высотой fINIT. По теории переходных состояний,
преодоление такого барьера и образование первого витка в данном месте цепи
происходит за время
| tINIT = t.exp(+fINIT /kT) , | (9.7) |
где t — время элементарного шага
(в данном случае — элонгации спирали на один остаток), а экспонента
учитывает малую населенность барьерного состояния. В силу уравнения (9.6)
| tINIT = t /s. | (9.8) |
Однако инициация может произойти
в любой точке спирали, а ее длина — порядка n0
=s -1/2. Значит,
характерное время инициации первого витка в каком-то месте будущей
спирали составляет в n0 раз меньше
времени, а tINIT/n0=
t/(n0s)
= t /s
1/2.
На то, чтобы уже инициированная
спираль охватила все свои ~n0 звеньев,
требуется потом примерно то же (что и на инициацию) время, ~tn0=
t/s
1/2. Значит, все время перехода клубок-спираль в полипептиде
должно составлять примерно
| ta = 2t /s1/2, | (9.9) |
и половина, грубо говоря, этого времени идет на инициацию спиралей в
разных местах цепи, а половина — на элонгацию, протекающую,
в согласии с предварительной оценкой, со скоростью порядка 1 остаток за
наносекунду.
Кинетика образования a-спиралей
относительно проста: они всегда образуются быстро. Кинетика образования
b-структуры много сложнее и интереснее.
b-структура
в полипептидах часто образуется очень медленно — за часы, а
бывает — за недели (хотя бывает, что и за миллисекунду). Почему?
И, в то же время, — белки с b-структурой
сворачиваются не медленнее a-спиральных белков.
Как они успевают? И что отвечает за аномалии в образовании b-структуры
в полипептидах — медленная инициация или медленная элонгация?
"Аномальная" (по сравнению с переходом
спираль-клубок) кинетика образования b-структуры
связана с тем, что она — двумерный (а не одномерный,
как спираль или клубок) объект (Рис.9-4).
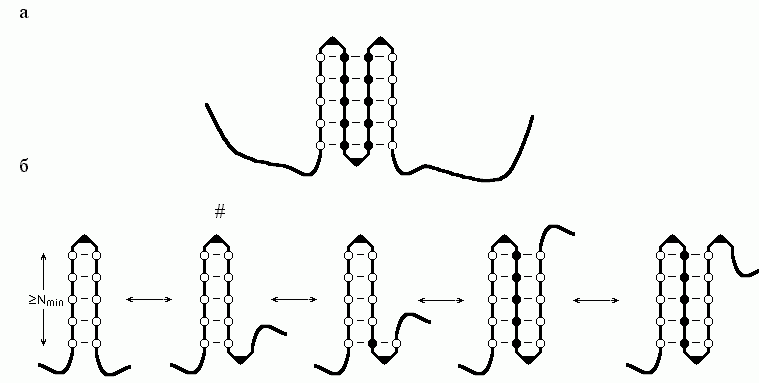
Рис.9-4. (а) Схема b-листа.
Аминокислотные остатки внутренних b-участков
показаны черными кружками, краевых b-участков
— пустыми кружками; изгибы (или петли), соединяющие b-участки,
изображены в виде уголков. (б) Описанный в тексте сценарий роста b-листа.
Самая нестабильная структура помечена значком #.
Находящиеся на краю листа звенья цепи имеют меньше контактов с другими, чем внутренние звенья листа. Иными словами, край b-листа (как и граница любой другой фазы — например, капли воды, льдинки или a-спирали) имеет повышенную свободную энергию. Однако — в отличие от a-спирали (и в сходстве с каплей) — b-лист не одномерен, т.е. размер его края (а значит, и его свободная энергия) растет с числом вовлеченных в этот лист звеньев цепи. Поэтому переход клубок — b-структура становится фазовым переходом первого рода — как образование капли или льдинки. Покажем, что из-за этого на пути образования b-листа возникает высокий (особенно при образовании лишь слегка стабильной b-структуры) свободно-энергетический барьер, который может в миллионы и миллиарды раз замедлить инициацию ее сворачивания.
Край b-листа
сложен из (а) краевых b-тяжей, и (б) изгибов
или петель, соединяющих все b-тяжи (Рис.9-4а).
Пусть свободная энергия клубка принята за 0 (т.е. за начало отсчета), fb
— свободная энергия остатка в центре b-листа,
fb+Dfb
— свободная энергия остатка на его краю (т.е. Dfb
— краевой эффект), и U — свободная энергия изгиба. Раз
b-лист вообще образуется — то он
стабилен (т.е. fb
<0), а краевые эффекты препятствуют его распаду на кусочки (т.е. Dfb>0
и U>0).
В кинетике образования b-структуры
надо различать два случая:
А) fb+Dfb<0,
т.е. длинная b-шпилька сама по себе стабильнее
клубка. Тогда только образование изгиба в вершине этой шпильки требует
преодоления активационного барьера (примерно такого же, как при образовании
a-спирали), а дальнейший рост b-структуры
идет быстро — примерно как элонгация a-спирали
(см. линию с fEL<0 на Рис.9-3).
Б) fb+Dfb>0,
т.е. b-шпилька сама по себе нестабильна, и только
прилипание к инициирующей b-шпильке последующих
b- тяжей стабилизует b-лист.
Активационному барьеру тогда соответствует образование "зародыша"
— такого b-листа или b-шпильки,
что дальнейший рост листа пойдет уже с общим понижением свободной энергии.
Образование и последующее "прорастание"
зародыша новой фазы — характернейшая особенность фазовых переходов
первого рода, к коим принадлежит и образование b-структуры.
Однако преодоление связанного с образованием зародыша активационного барьера,
как мы скоро убедимся, может быть очень и очень медленным.
Рассмотрим следующий простейший
сценарий роста стабильного b-листа (Рис.9-4б):
образование инициирующей b-шпильки из изгиба
и двух b-тяжей, по N звеньев (аминокислот) в
каждом; образование последующего изгиба на ее конце; прилипание к листу
b-тяжа из N звеньев; образование последующего
изгиба; прилипание b-тяжа; и так далее.
Возникновение — из
клубка — b-шпильки из изгиба и двух
N-звенных b-тяжей повышает свободную энергию
цепи на U+2N(fb+Dfb);
образование последующего b-изгиба повышает ее
еще на U. Прилипание к N-звенному краю этой шпильки N-звенного b-тяжа
снижает свободную энергию на Nfb
(ведь при этом число краевых звеньев не меняется, а число внутренних растет
на N); образование последующего b-изгиба опять
повышает свободную энергию на U; прилипание нового N-звенного b-тяжа
снова понижает ее на Nfb,
и т.д.
Цикл "прилипание нового b-тяжа
и образование нового b-изгиба" изменяет суммарную
свободную энергию на Nfb+U.
А так как в результате такого цикла свободная энергия должна снижаться
(только тогда сворачивание цепи пойдет быстро), то прилипающий b-тяж
(а равно и тот, к которому он прилипает) должен состоять не менее чем из
Nmin = U/(-fb)
звеньев.
"Переходным", т.е. самым нестабильным
состоянием по ходу образования b-структуры является
(по нашему сценарию) b-шпилька с последующим
изгибом. Так как стабильность шпильки падает с удлинением, а b-тяж
в инициирующей шпильке должен состоять как минимум из Nmin
звеньев, то минимальная свободная энергия инициирующей b-шпильки
составляет
| F# = U+2Nmin(fb+Dfb)+U = 2(UDfb)/(-fb). | (9.10) |
Это — свободная энергия переходного состояния при образовании b-листа по нашему сценарию. Теперь осталось только показать, что, какой сценарий ни возьми, существенно более стабильных переходных состояний быть не может.
Чтобы показать это —
оценим, как будет меняться минимальная свободная энергия b-листа
с его увеличением. Общий ход изменения показан на Рис.9-5. Пока лист мал,
доминируют краевые эффекты, и свободная энергия повышается. В большом же
листе доминируют внутренние остатки, и его свободная энергия падает.
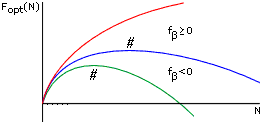
Рис.9-5. Общий ход изменения
Fopt, минимальной свободной энергии b-листа,
с увеличением числа М звеньев в нем. Кривые относятся к разным свободным
энергиям fb
внутренних звеньев b-листа. # —
точка максимума величины Fopt по ходу роста
b-листа. При росте b-листа
(в отличие от роста a-спирали, см. Рис.9-3)
максимум его свободной энергии не приходится на самое начало этого процесса.
Теперь перейдем к расчетам. Сначала
оценим минимальную свободную энергию M-звенного b-листа.
Свободная энергия листа, состоящего из m b-тяжей
(равной длины, чтобы минимизировать краевую свободную энергию) и m-1 изгиба,
равна
| F(M,m) = Mfb + 2(M/m)Dfb + (m-1)U | (9.11) |
Варьируя число b-участков
m, найдем минимум этой свободной энергии из условия
| dF/dm = -2(M/m2)Dfb + U = 0. | (9.12) |
Отсюда следует оптимальное число
b-участков в этом листе, mopt
= M1/2 [2Dfb/U]1/2 и
его свободная энергия, Fopt(M)
= F(M,mopt) = Mfb
- U + 2 M1/2 [2Dfb.U]1/2.
Варьируя величину Fopt(M) по M, находим
ее максимум (см. Рис.9-5) из условия
| dFopt/dM = fb + M-1/2 [2Dfb.U]1/2 = 0. | (9.13) |
Далее можно определить размер b-листа,
соответствующего этому максимуму, M*
= 2(Dfb.U)/(-fb)2, и его свободную энергию
| F* = Fopt(M* ) = 2(Dfb.U)/(-fb) — U. | (9.14) |
Величины F*
и F# (см. формулу 9.10) совпадают в главном
члене, 2(Dfb.U)/(-fb).
Именно из-за него свободная энергия перех![]() дного
состояния F# всегда велика, когда
свободная энергия стабилизации b-структуры (-fb)
мала, т.е. когда b структура находится на грани
стабильности. В сущности, F# стремится
к бесконечности, когда b структура приближается
к термодинамическому равновесию с клубком, т.е. когда (-fb)
® 0.
дного
состояния F# всегда велика, когда
свободная энергия стабилизации b-структуры (-fb)
мала, т.е. когда b структура находится на грани
стабильности. В сущности, F# стремится
к бесконечности, когда b структура приближается
к термодинамическому равновесию с клубком, т.е. когда (-fb)
® 0.
Так как, согласно теории переходного
состояния, время процесса t зависит от свободной энергии переходного (самого
нестабильного промежуточного) состояния F#
как
| tb ~ tb.exp(+F#/kT), | (9.15) |
где tb
— время элементарного шага (в данном случае — элонгации
b-листа на один остаток; и нет причин, чтобы
скорость элонгации b-листа качественно отличалась
бы от скорости элонгации спирали), то характерное время образования b
листа, при малых -fb,
есть
| tb ~ tb.exp[A/(-fb)] , | (9.16) |
где A — некая константа. Каково бы ни было ее численное
значение, — видно (см. Рис.9-6), что при малых -fb
время образования b структуры будет огромно
(в пределе — бесконечно велико).
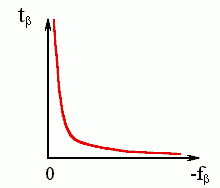
Рис.9-6. Общий вид зависимости
характерного времени образования b-листа от
стабильности b-структуры.
Итак: малостабильная b-структура
(а именно она наблюдается в неагрегирующих полипептидах) должна образовываться
очень медленно, — и причина здесь не в медленной элонгации,
а в медленной инициации — трудно собрать свободную энергию
из теплового движения и преодолеть высокий барьер.
Так объясняется и экспериментально наблюдаемая, очень медленная скорость
образования b-структуры в неагрегирующих полипептидах, и резкий ее рост
с повышением стабильности b-структуры.
В то же время стабильные b-листы
и шпильки (а именно они и наблюдаются в белках) должны образовываться довольно
быстро — примерно как a-спираль.
Крайне медленная инициация
— общее свойство фазовых переходов первого рода, когда возникающая
фаза находится на грани стабильности. Вспомните: переохлажденная жидкость,
перегретый пар... Все это связано с большой свободной энергией обширной
граница раздела фаз. А b-структура как раз и
образуется фазовым переходом первого рода — со всеми
вытекающими последствиями...
Наоборот, a-спираль
не образуется фазовым переходом первого рода [вспомните: граница
спирали, в отличие от границы b-структуры (или
льдинки), не растет с ее размером] — поэтому барьер,
который нужно преодолеть при сворачивании спирали, всегда имеет конечную
(и небольшую) величину, и она может успеть "проинициироваться" за микросекунду.
Заключительное замечание: что такое
"клубок". Этим термином я много раз пользовался, говоря о цепи,
не имеющей определенной структуры. Действительно, клубок не имеет никакого
дальнего порядка — что, однако, не исключает слабый (на масштабе
всего нескольких подряд идущих звеньев цепи) ближний порядок.
Самой интересной особенностью
клубка (экспериментально наблюдаемой с помощью гидродинамических методов,
при помощи рассеяния света и рентгеновских лучей) является его крайне малая
плотность и совершенно особая зависимость его размеров — радиуса
и объема — от длины цепи.
Для выяснения этой особенности,
рассмотрим простейшую модель клубка, так называемую "свободно-сочлененную
цепь" (Рис.9-7). Она состоит из звеньев-"палочек"; "звено" может включать
в себя несколько мономеров полимерной цепи; главное — что каждая
"палочка" может свободно, как угодно поворачиваться в сочленении относительно
своих соседей по цепи. Пусть в цепи M "палочек", и длина каждой равна r.
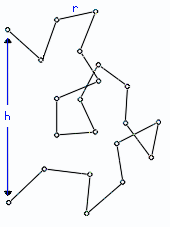
Рис.9-7. Свободно-сочлененная
цепь — модель клубка.
Такую цепь можно описать как цепочку
из векторов r1, r2
,..., rM (напомню: вектор в математике
— это отрезок прямой, имеющий направление). Эти вектора имеют одинаковую
длину r, и каждый из них направлен от предыдущего сочленения к последующему.
Сумма векторов
| (9.17) |
есть просто вектор, идущий от начала к концу цепи. Квадрат длины этого
вектора есть
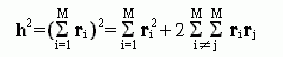 |
(9.18) |
Найдем теперь среднюю величину
<h2>, т.е. усредним h2
по всем возможным тепловым флуктуациям цепи. При этом мы должны учесть,
что <ri2>, средний
квадрат вектора ri, есть просто
r2, а среднее произведение любых векторов
<rirj>
есть 0 при i№j, так как, свободно вращаясь,
эти вектора имеют ту же вероятность быть направленными что в одну, что
в разные стороны.
Значит, средний квадрат расстояния
между концами свободно-сочлененной цепи есть
|
|
(9.19) |
то есть линейные размеры (радиус и т.д.) клубка растут с ростом числа
M звеньев в цепи как M1/2. Отсюда следует,
что объем клубка пропорционален M3/2
— в то время как для всех "нормальных" (имеющих фиксированную плотность)
тел объем растет только как число частиц M, — т.е. гораздо
медленнее, чем M3/2. Такая аномально сильная
зависимость объема клубка от размера цепи и есть самое характерное свойство
клубка. Из него, в частности, вытекает крайне низкая плотность клубка,
образованного длинными цепями, и, как следствие — практическое
отсутствие контактов между дальними по цепи звеньями.
Недостаток, недостаточная реалистичность
свободно-сочлененной модели — в том, что она рисует клубок
в сильно идеализированном виде, т.к. допускает, что в любом своем звене
цепь может поворачиваться на любой угол, — а это, вообще говоря,
не так. Однако формулу (9.19) можно переписать в более общем виде,
| <h2> = Lr , | (9.20) |
где L = Mr — полная ("контурная") длина цепи, пропорциональная
числу звеньев в ней, а r —
эффективное расстояние между "свободными сочленениями" цепи, т.е. характерная
длина, на которой цепь "забывает" о своем направлении (для справки: в полипептидной
цепи эта характерная длина — или, как говорят, "длина Куновского
сегмента" — составляет 30 — 40![]() ,
т.е. Куновский сегмент такой цепи содержит около 10 аминокислотных остатков).
В виде (9.20) формула, описывающая размер клубка, уже обретает достаточную
общность и может применяться для описания реальных полимеров.
,
т.е. Куновский сегмент такой цепи содержит около 10 аминокислотных остатков).
В виде (9.20) формула, описывающая размер клубка, уже обретает достаточную
общность и может применяться для описания реальных полимеров.